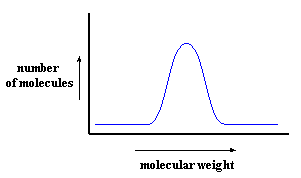
La première façon d'obtenir un tel diagramme est d'utiliser la chromatographie d'exclusion, ou SEC. Mais la SEC ne mesure pas réellement le poids moléculaire. Elle mesure le volume hydrodynamique, c'est la taille de la chaîne du polymère enroulé sur elle même dans la solution. Ceci donne une mesure relative de la masse moléculaire car, évidemment, plus la masse moléculaire est élevée plus le volume hydrodynamique est élevé.
Il arrive que l'on aie besoin de savoir exactement quelle est la distribution du poids moléculaire. Il a donc été laissé le soin à quelques scientifiques intelligents d'inventer quelque chose que l'on appelle désorption laser assistée par matrice ou spectro de masse MALDI pour faire plus court. Quelques fois quand nous sommes vraiment paresseux on l'appelle juste MALDI.
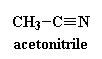 Donc quelle est cette chose fantastique appelée MALDI? Pour l'expliquer,
nous allons parcourir le procédé MALDI et voir comment il se
déroule. Premièrement, nous prenons notre polymère et
nous le dissolvons dans un solvant. Quelle sorte de solvant? eh bien, cela
dépend. Les premières manipulations de MALDI ont été
faite sur des protéines. Les protéines
sont solubles dans l'eau et donc l'eau à été le premier
solvant. Il est courant d'utiliser un mélange 70:30 d'eau et d'acetonitrile
(cliquez dessus pour le voir en 3D). Le solvant que l'on utilise dépend
de quel solvant dissous le polymère que vous étudiez.
Donc quelle est cette chose fantastique appelée MALDI? Pour l'expliquer,
nous allons parcourir le procédé MALDI et voir comment il se
déroule. Premièrement, nous prenons notre polymère et
nous le dissolvons dans un solvant. Quelle sorte de solvant? eh bien, cela
dépend. Les premières manipulations de MALDI ont été
faite sur des protéines. Les protéines
sont solubles dans l'eau et donc l'eau à été le premier
solvant. Il est courant d'utiliser un mélange 70:30 d'eau et d'acetonitrile
(cliquez dessus pour le voir en 3D). Le solvant que l'on utilise dépend
de quel solvant dissous le polymère que vous étudiez.
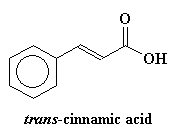
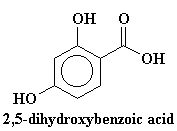
Nous additionnons aussi un ingrédient spécial. C'est un composé du genre acide trans-cinnamic ou acide 2,5-dihydroxybenzoic . Ceci dépend de chaque polymère, mais l'important c'est que cet ingrédient spécial absorbe la lumière dans l'ultraviolet. Habituellement on ajoute 104 fois plus d'absorbeur d'UV que de polymère.
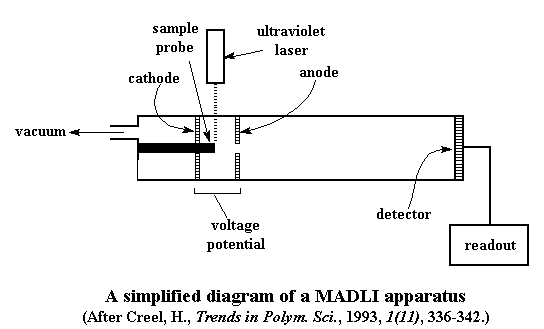
Quelqu'un a dit laser? C'est vrai, il nous faut maintenant tirer au laser sur notre échantillon. Cela n'est peut être pas très passionnant pour vous les plus jeunes, mais pour nous des personnes plus âgées qui ont grandies avant que les lasers aient été omniprésents ceci est plutôt extraordinaire. Nous utilisons habituellement un laser ultraviolet dans la gamme de 330-360 nm. Rappelez-vous que notre échantillon est mélangé avec le matériau UV-absorbant. Il aime la lumière UV, et ne peut pas obtenir assez de lui. Ainsi il absorbe toute l'énergie qu'il peut du laser. Naturellement, il transmet également une partie de cette énergie aux molécules de polymère.
Le matériaux de la matrice réagit également avec des polymères de telle manière que les polymères deviennent des ions chargés. Personne ne sait vraiment comment ceci se produit. Le fait que les polymères soient maintenant ioniques sera très important juste après.
Mais d'abord voyons ou passe toute cette énergie que les polymères absorbent. Quand elles l'absorbent certaines des molécules de polymère font quelque chose que les polymères ne font presque jamais. Elles s'évaporent. Habituellement les molécules de polymère sont trop grandes et lourdes pour s'évaporer, mais à ces températures élevées, et ces basses pressions, elles peuvent le faire. C'est là d'où vient le mot désorption dans le nom.
Maintenant que nous avons nos polymères flottant à l'état gazeux, il est temps que je vous dise quelque chose d'important au sujet de cette chambre. À l'extrémité de la chambre où nous évaporons nos molécules de polymère nous avons deux électrodes, une cathode positive, et une anode négative. Selon le genre de polymère et le genre de matériau de matrice que vous employez, les polymères peuvent être des cations ou des anions. Pour cette explication nous dirons le polymère que nous regardons forme des cations positifs.
Maintenant quand nous vaporisons notre polymère, nous le vaporisons juste entre les deux électrodes. Quand notre polymère forme des cations, nous plaçons la cathode derrière l'échantillon, et l'anode négative devant l'échantillon. (Jetez encore un coup d'oeil au diagramme.) Naturellement, les polymères chargés vont dans la direction de l'anode, attirée par sa charge négative. Si nous l'utilisons correctement, nous pouvons employer cette accélération pour tirer les molécules de polymère jusqu'au détecteur à l'extrémité de la chambre.
La majeure partie du temps, il y a seulement une charge positive sur chaque molécule de polymère. Ceci signifie que la même force électrique est appliquée sur chaque molécule de polymère quand elle est accélérée dans le champ électrique entre les deux électrodes. Mais rappelez-vous, les molécules de polymère ont des masses différentes.
Qu' a dit Isaac Newton au sujet de la masse, de la force, et de l'accélération? Je pense que c'est quelque chose comme ceci:
F = ma
c'est-à-dire, la force est égale à la masse que multiplie l'accélération. Mais nous pouvons réarranger l'équation comme ceci:
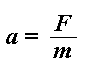
Ainsi, comme vous l'avez compris, pour une force donnée, plus il y a de masse, plus l'accélération est faible. Pour nous ceci signifie que les grandes molécules lourdes de polymère prendront beaucoup plus longtemps pour atteindre le détecteur à l'extrémité de la chambre.
Ainsi les polymères frapperont le détecteur, les petits d'abord, puis les grands. Ils frappent exactement par ordre de masse. Toutes les molécules de polymère du même poids moléculaire frapperont le détecteur ensemble. Quand elles frappent le détecteur, le détecteur enregistre une crête. La taille de la crête est proportionnelle au nombre de molécules qui frappent en même temps. Ainsi quand nous aurons fini nous obtiendrons une série de crêtes qui ressemble à ceci:
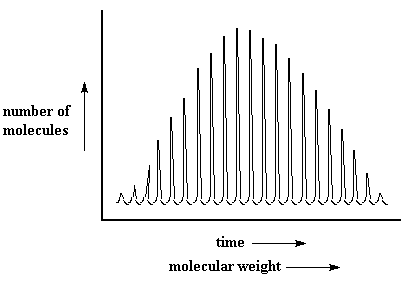
Je ne sais pas vous, mais ce spectre de MALDI m'a toujours rappelé l'aileron géant sur le dos d'un dimetredon, un reptile éteint qui a vécu il y a des millions d'années.

MALDI et SEC
Un petit détail que vous pouvez noter est que le poids moléculaire augmente de gauche à droite sur ce graphique. Sur un graphique SEC que vous voyez plus souvent, le poids moléculaire augmente de droite à gauche. (vous savez pourquoi maintenant?) Ceci peut porter à confusion parfois, gardez-le à l'esprit.
Mais il y a des différences plus importantes entre la sec et MALDI. La sec vous donne une distribution approximative du poids moléculaire . La sec mesure le volume hydrodynamique, et non le poids moléculaire. Nous pouvons entre alors approximer le poids moléculaire, en comparant le volume hydrodynamique du polymère que nous avons examiné à un standard, habituellement le polystyrène, pour lequel nous savons le rapport exact entre le volume hydrodynamique et le poids moléculaire. Ceci donne seulement un résultat approximatif parce que le rapport le poids moléculaire et le volume hydrodynamique n'est pas toujours le même pour chaque polymère.
Mais MALDI mesure la masse plus exactement, parce qu'il ne compare pas le polymère que vous mesurez à quelque chose. Il donne une mesure absolue de la masse. La spectro MALDI remplacera probablement la sec dans la plupart des laboratoires.

